在新的安全审查后,加拿大卫生部与非那雄胺制造商合作加强对自杀倾向的警告
2023年3月27日
亲爱的朋友们:
尽管美国食品和药物管理局很少提及非那雄胺后综合征(PFS),但其副作用数据库充分说明了这种疾病的流行。
根据部分基于该机构不良事件报告系统(FAERS)的最新研究,使用非那雄胺导致抑郁和焦虑的可能性平均是两种对照药物的23倍:与抑郁症有关的β-受体阻滞剂Inderal和用于治疗脱发的保钾利尿剂Spironolactone。
同样,使用非那雄胺导致失眠、疲劳、自杀倾向和自杀的可能性达9倍。
题为《非那雄胺的神经精神反应:反安慰剂还是真实效果?》的1100字论文由耶路撒冷希伯来大学医学名誉教授Mayer Brezis博士发表在上个月的《基础与临床药学杂志(Journal of Basic and Clinical Pharmacy)》上。
Brezis博士写道:
越来越多的不良反应报告表明,即使在停药后,非那雄胺也可能导致抑郁、焦虑、自杀倾向和性功能障碍。另一方面,一些出版物声称,这可能代表了反安慰剂效应的模拟报告。在本论文中,我们……证明了非那雄胺的安全信号显著不相称。
此外,在过去十年中,非那雄胺引起的神经精神反应的增加与FDA报告的与该药物有关的自杀事件的显著增加是一致的。
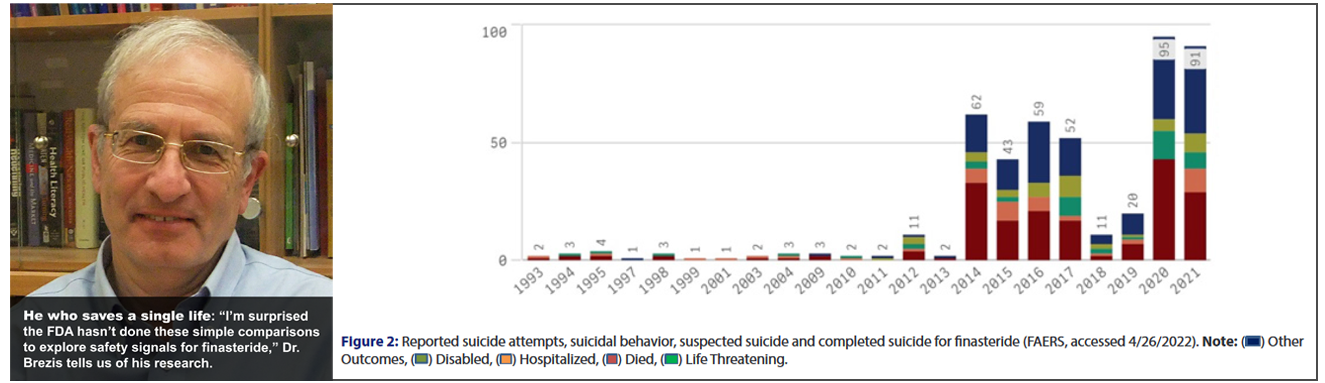
通过不良事件报告系统(FAERS),Brezis博士查阅了1993年至2021年涉及非那雄胺的自杀数据,其中包括自杀未遂、自杀行为、疑似自杀和完成自杀的报告,其结果包括:死亡、残疾、住院以及危及生命等等。
此类报告的绝对数量在2020年达到顶峰,为95例,2021年仅下降4%,至91例。然而,从2019年到2020年,这类事件的数量上升了375%。
更引人注目的是十年来的数据。 2010 年,FAERS 仅包含两份非那雄胺自杀率报告,到 2020 年,自杀率将上升 4,650%。2001 年,FAERS 仅包含一份非那雄胺自杀率报告,到 2021 年,自杀率将上升 9,000%。
Brezis博士还指出:
由于自杀与反安慰剂效应无关,看来我们很可能正面临着非那雄胺对情绪的真实而严重的不良影响。报告数量的增加可能与意识的增强有关,而非与反安慰剂效应有关。
对PFS患者来说,被打上疯子的烙印并不是什么新鲜事
在PFS基金会的约3000个主动病例报告数据库中,约有400名(13%)患者投诉说医生将这种疾病定性为心身疾病。例如:
2019年,来自加州洛杉矶的22岁的JB写道:
我一个月前开始服用非那雄胺,然后就感觉完全不像我自己了,自杀想法和焦虑都不断涌上心头。我的心感到冰冷和无情。我平时热衷于的事情,比如和粉丝直播互动,现在似乎对我没什么吸引力……我经常无法勃起……医生一直告诉我,实际上没有人患有PFS……这都是我的幻觉。
2017年,来自葡萄牙Setúbal的AA,时年26岁,他写道:
我不抽烟,不喝酒,不吸毒,不嗑药,练习游泳等。我是一名呼吸生理学者,我每天服用1毫克非那雄胺,坚持了两年。现在,我遇到了前列腺炎、尿流量小、阴茎麻木、生殖器萎缩、零性欲、极度脑雾、极度极度疲劳、失眠、有自杀念头等副作用。我咨询过一些泌尿科医生、内分泌科医生和皮肤科医生等,他们都不理会我的病情。他们说这都是我脑子里臆想出来的……我再也等不到治愈了。我要在短时间内结束自己,一了百了。
与这些投诉几乎同时发表的两篇皮肤科医生的研究论文,加剧了医疗服务提供者的冷漠和患者的痛苦:
- 5-α-还原酶抑制剂综合征的合理性调查。皮肤附件疾病:Raymond Fertig,医学博士,迈阿密大学米勒医学院,2016年。
Fertig博士写道:
在被告知服用非那雄胺可能有副作用的患者中,存在明显的安慰剂/反安慰剂效应,这可能解释了报道的性功能障碍的高流行性,包括参与互联网小组和博客的受试者的持续性功能障碍。
- 非那雄胺后综合征:一种诱发型妄想障碍,有可能成为一种群体性心因性疾病?皮肤附件疾病:Ralph M. Trüeb,医学博士,苏黎世大学,2019年。
Trüeb博士写道:
PFS的概念来自于非皮肤科医生的报告、神经内分泌学的研究和反思,以及低质量且具有强偏倚选择的不受控研究,而在得知非那雄胺可能副作用的患者中存在显著的反安慰剂效应是公认的。
远程医疗公司暗示道,这一切都在你的头脑中
最近,世界第五大远程医疗公司进一步提出PFS可能只是反安慰剂效应导致。
在Hims & Hers Health (NYSE: HIMS)目前提供的数字消费者内容中,有一个页面名为“非那雄胺后综合征:它是什么?”这篇2700字的博客文章由Hims的编辑团队撰写,由执业护士Kate Hagerty进行了“医学审查”,最后一次更新是在2021年10月。下面是其中一些段落:
- 在医学界,关于“非那雄胺后综合征”是一种真实的医疗疾病还是一种心理疾病存在争议……专家认为,通常被描述为“非那雄胺后综合征”的症状可能由几种不同的因素引起。
- 第一个因素是反安慰剂效应。这是一种心理现象,它是指一个人对特定药物或治疗的负面预期可能会导致他们经历负面的症状。
- 第二个可能解释[PFS]症状的因素是现有精神疾病……研究人员从理论上推断,报道的[PFS]症状可能不是由非那雄胺本身引起的,而只是偶然与使用非那雄胺有关。
所有的指责都指向FDA未能警告公众,因30年前批准的一种药物导致了异常的自杀激增,而我们更期待在不久的将来出台更严格的监管规定。
因为就在10天前,该机构在首次公开提及这种疾病时,公布了即将举行的患者倾听会议的主题,其中之一是非那雄胺后综合征。
2018年设立的FDA患者倾听会议(PLS):
- 是小型、非正式、非监管、非公开的电话会议,允许参与者与FDA工作人员直接联系。
- 主要涉及患者的经历、看法和与他们的健康或疾病相关的需求,而非特定的医疗产品(药物、生物制剂或设备)。
- 让FDA有机会与弱势群体建立联系。
他们的目标包括:
- 教FDA审查人员了解对患者、护理人员、倡导者和社区代表很重要的疾病、症状以及与健康相关的经历和看法。
- 通知有关例如针对特定产品或应用、好处/风险权衡以及制定指南的监管决策。
- 帮助提供一个指导或加速早期研究和开发的出发点,例如,帮助确定终点和新的结果评估工具。
在每次倾听会议 (可以是应FDA要求,也可以是患者主导)之后,鼓励患者管理人员对活动进行总结。一旦该总结被FDA审查,它就会发布在该机构的患者倾听会议(PLS)总结页面上。
敬请期待PFS总结,我们相信它将使我们的联邦政府更接近于承认非那雄胺后综合征是由非那雄胺引起的。
加拿大进一步打击非那雄胺后综合征
与美国形成鲜明对比的是,加拿大十多年来一直在积极监测非那雄胺与自杀的潜在联系,并将其调查结果公之于众。加拿大卫生部(HC)、国家药品监管机构(DRA),在2012年完成了第一次非那雄胺安全性审查,随后在2015年完成了第二次审查。
 但直到2019年的第三次审查,加拿大卫生部才发现流行病学信号已经强到足以采取行动;即,更新非那雄胺产品标识(在美国称为产品标签),以加入自杀意念的风险。
但直到2019年的第三次审查,加拿大卫生部才发现流行病学信号已经强到足以采取行动;即,更新非那雄胺产品标识(在美国称为产品标签),以加入自杀意念的风险。
现在是第四次审查,加拿大卫生部表示这是由美国的媒体报道引发的。
该审查于2022年进行,目的是“考虑最近的信息,并确定是否有必要采取进一步措施”。
部分调查结果如下:
- 加拿大卫生部审查了加拿大警戒(Canada Vigilance)数据库中有关使用非那雄胺的401例自杀、自杀意念和/或自伤患者。在401例病例中,25例符合进一步评估的标准,从而确定使用非那雄胺与自杀、自杀意念和自伤之间是否存在联系。
- 在25例病例中,发现23例可能与使用非那雄胺有关。
- 在25例患者中,有17例患者年龄在40岁或以下,并服用非那雄胺治疗男性型脱发。
- [加拿大卫生部]还审查了科学文献中的16篇出版物。关于使用非那雄胺与自杀、自杀意念和自伤风险之间的关联,有越来越多的科学证据。
因此,与法国同行法国国家药品和保健品安全检测局(ANSM)最近采取的措施非常一致,加拿大卫生部报告称:
- 正在与制造商合作更新含非那雄胺产品的产品安全信息,以加强关于自杀意念和自残风险的警告声明,并加入在开始治疗前筛查患者精神风险因素的信息,以及在治疗期间和停止治疗后持续监测患者。
- 还将通过Health Product InfoWatch将这一更新告知医疗保健专业人员。
(有关其他国家如何监测非那雄胺不良事件、向公众披露风险和监管药物的信息,请参阅我们的PFS全球预警地图。)
路透社救场
 加拿大卫生部表示,引发其第四次安全审查的媒体报道是源于对非那雄胺制造商默克公司(NYSE: MRK)长达一年的渎职调查。
加拿大卫生部表示,引发其第四次安全审查的媒体报道是源于对非那雄胺制造商默克公司(NYSE: MRK)长达一年的渎职调查。
2019年9月,路透社发表了一篇3900字的调查报告,题为《法院允许默克公司隐瞒一种流行药物的风险》。这篇由Dan Levine撰写的报道揭露了默克公司前高管在美国保法止诉讼案中的证词,这些证词表明默克公司在临床试验期间淡化了非那雄胺的副作用。
报道曝光后的第二天,路透社向美国联邦法院提交了一项动议,要求解密保法止诉讼中提交的文件,并指出:“这是一个非常重要的案件,却被封存了,而且没有记录在案的发现来解释封存的原因。第一修正案反对这种结果。”
2021年1月,美国地方法官Peggy Kuo批准了路透社的动议,为公开保法止诉讼文件扫清了道路。
10天后,据路透社报道,一篇题为《默克公司抗谢顶药物保法止涉及大量自杀报告》的报道显示:
默克公司和美国监管机构知道男性服用保法止会有自杀行为,但他们却决定在2011年更新标签时不警告消费者这些潜在风险,自2011年做出警告决定以来,FDA已经收到了700多份服用该药物的人自杀和有自杀想法的报告。其中至少有100例死亡。在此之前,在该药物上市的前14年里,该机构收到了34份此类报告,其中包括10例死亡。
在此之后,加拿大开始再次深入研究PFS的盛行。
 任何居住在美国并患有非那雄胺后综合征的人都应该向美国FDA报告其症状。任何居住在美国以外并患有非那雄胺后综合征的人都应该向美国FDA以及其当地的药品监管机构报告其症状,正如我们的“举报你的副作用/Report Your Side Effects”页面所示的那样。
任何居住在美国并患有非那雄胺后综合征的人都应该向美国FDA报告其症状。任何居住在美国以外并患有非那雄胺后综合征的人都应该向美国FDA以及其当地的药品监管机构报告其症状,正如我们的“举报你的副作用/Report Your Side Effects”页面所示的那样。
最后,如果您或您爱的人正在遭受非那雄胺后综合征,特别是感到抑郁或情绪不稳定,请不要犹豫,尽快通过我们的患者支持热线联系我们:social@pfsfoundation.org
谢谢!