“Todavía no está claro en qué medida la menor exposición sistémica al fármaco se traduce en un menor riesgo de efectos secundarios”, dice Deutsche Apotheker Zeitung. «El número limitado de pacientes crea dificultades en sacar conclusiones fiables».
20 de marzo de 2023
Queridos amigos:
La revista farmacéutica más antigua y más leída de Alemania se ha sumergido profundamente en el síndrome post-finasteride (PFS).
 Eso, en un esfuerzo por brindar a sus 29,000 suscriptores la información más científicamente sólida sobre la finasterida tópica no aprobada por la FDA.
Eso, en un esfuerzo por brindar a sus 29,000 suscriptores la información más científicamente sólida sobre la finasterida tópica no aprobada por la FDA.
Eso, también, antes de que otra nación saque al mercado la finasterida tópica como una alternativa «más segura» a el medicamento oral.
Mañana, la empresa farmacéutica coreana Boryung (003850.KS), con la bendición del Ministerio de Seguridad de Alimentos y Medicamentos, lanzará el spray de finasterida Finjuve en la República de Corea. Fabricado por Hikma Pharmaceuticals (LSE: HIK), con sede en el Reino Unido, Finjuve ya está aprobado en Alemania, Italia, Portugal y Luxemburgo.
Debida diligencia
Efectos Secundarios: Crecimiento del cabello y sus consecuencias (resumen inglés), el metanálisis de 2000 palabras realizado por Tony Daubitz, PhD, se publicó el 10 de marzo en Deutsche Apotheker Zeitung (DAZ), solo un mes después de su primer informe sobre el tema: Finasteride tópico, ¿una mejor alternativa para tratar la alopecia? (Inglés).
En total, el Dr. Daubitz, quien obtuvo su doctorado en el Centro Max Delbrück de Medicina Molecular en Berlín, cita 28 estudios clínicos, muchos de cuyos autores son sin duda familiares para los lectores de esta fuente de noticias, entre ellos:
Roberto Cosimo Melcangi, PhD, de la Universidad de Milán, Mohit Khera, MD, de Baylor College of Medicine, Michael S. Irwig, MD, de Harvard Medical School y Abdulmaged M. Traish, PhD, de Boston University School of Medicine.
También proporciona el cuadro a continuación de 17 síntomas de PFS de informes de casos publicados:
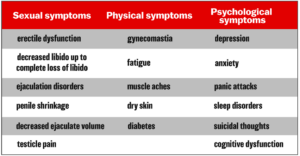 Después de presentar evidencia que respalda la hipótesis de que una proporción de todos los pacientes que toman finasterida oral desarrollan PFS, el Dr. Daubitz escribe:
Después de presentar evidencia que respalda la hipótesis de que una proporción de todos los pacientes que toman finasterida oral desarrollan PFS, el Dr. Daubitz escribe:
Una nueva alternativa de tratamiento [a la finasterida oral] es la finasterida tópica (Fynzur, 2275 mg/ml), que se lanzó recientemente en Alemania. En un estudio de fase III con 250 voluntarios [Eficacia y seguridad de la solución en aerosol de finasterida tópica para la alopecia androgenética masculina], el aerosol estimuló significativamente el crecimiento del cabello… y mostró efectos similares a los de la finasterida oral… Por otro lado, la exposición sistémica al fármaco con la aplicación dérmica fue menos de una centésima parte de la aplicación oral. Los niveles de DHT en la sangre también cayeron correspondientemente menos… por lo que se esperan menos efectos secundarios.
Proceda con extrema precaución
Entonces, la finasterida tópica es más segura, ¿verdad? Fin de la historia, ¿verdad? Difícilmente, escribe el Dr. Daubitz:
Lo que suena prometedor a primera vista aparece bajo una luz diferente a través de un análisis de la droga. No es posible decir si el efecto de la solución tópica es realmente equivalente al de la tableta, ya que el estudio no fue diseñado para evaluar estadísticamente este punto final. Y eso es solo el comienzo de sus deficiencias. Solo el 71% de los sujetos completaron el estudio y solo el 55% de los sujetos tenían fotos evaluables para evaluar el éxito de la terapia.
En un análisis de respuesta encargado por el [Instituto Federal de Medicamentos y Dispositivos Médicos], también se pidió a los sujetos que calificaran la mejora en el crecimiento de su cabello. Sin embargo, no hubo diferencias significativas en la valoración subjetiva (mejoría del crecimiento del pelo en el 39,8% de los hombres con finasterida tópica, el 31,0% con finasterida oral y el 32,0% con placebo).
Luego concluye:
Todavía no está claro en qué medida la menor exposición sistémica al fármaco se traduce en un menor riesgo de efectos secundarios. Aunque los efectos secundarios sexuales no se informaron con mayor frecuencia que con el placebo… el número limitado de pacientes en el estudio, como lo señaló Arznei-Telegramm, dificulta sacar conclusiones confiables. Sin embargo, es importante anticipar la aparición de tales efectos secundarios.
La creciente infamia de Hims
Después de presentar evidencia que respalda la hipótesis de que una proporción de todos los pacientes que toman finasterida oral desarrollan PFS, el Dr. Daubitz escribe:
Una nueva alternativa de tratamiento [a la finasterida oral] es la finasterida tópica (Fynzur, 2275 mg/ml), que se lanzó recientemente en Alemania. En un estudio de fase III con 250 voluntarios [Eficacia y seguridad de la solución en aerosol de finasterida tópica para la alopecia androgenética masculina], el aerosol estimuló significativamente el crecimiento del cabello… y mostró efectos similares a los de la finasterida oral… Por otro lado, la exposición sistémica al fármaco con la aplicación dérmica fue menos de una centésima parte de la aplicación oral. Los niveles de DHT en la sangre también cayeron correspondientemente menos… por lo que se esperan menos efectos secundarios.
Nunca se escribieron palabras más verdaderas. El mes pasado revelamos que, hasta la fecha, 12 pacientes con PFS nos han presentado informes de casos que indican que desarrollaron la afección después de usar solo finasterida tópica (Topical Finasteride Could Precipitate PFS, Top German Rx Journal Warns).
El primer caso que se hizo público fue el de Sumair Ahluwalia, un estudiante universitario de 21 años de Chicago, que desarrolló PFS en toda regla poco después de que Charlene Fernandez, enfermera practicante de Hims, le recetó el spray tópico de finasterida y minoxidil.
La referencia del Dr. Daubitz a Hims & Hers Health (NYSE: HIMS) marcó la segunda vez en tantos meses que Telemed, con sede en San Francisco, que también comercializa finasterida oral y tópica en el Reino Unido, fue destacada en los informes de los medios europeos.
El 4 de marzo, The Daily Mail publicó una historia titulada Watchdog lanza una investigación sobre la píldora para la caída del cabello, ya que los hombres informan un gran aumento de los efectos secundarios, que incluyen depresión, libido baja y disfunción eréctil. Su subtítulo decía: Las cifras muestran los efectos secundarios de los medicamentos para la caída del cabello vendidos bajo marcas como Hims en ascenso.
 Para nosotros, la incidencia cada vez mayor de pacientes con finasterida que reportan desarrollar PFS después de que Hims u otros telemédicos les recetaron el medicamento, es un punto de datos que hemos estado registrando durante cinco años. Como señalamos en nuestro discurso anual de 2018:
Para nosotros, la incidencia cada vez mayor de pacientes con finasterida que reportan desarrollar PFS después de que Hims u otros telemédicos les recetaron el medicamento, es un punto de datos que hemos estado registrando durante cinco años. Como señalamos en nuestro discurso anual de 2018:
Keshav Narain, cirujano oftalmólogo en San José, CA, nos escribió: “Hace poco vi a un paciente que tomaba finasterida… La obtuvo sin receta, a través de Hims. Creo que la gran mayoría de estas personas no tienen idea de los peligros potenciales de este medicamento. Además de los efectos secundarios conocidos que resultan del bloqueo de andrógenos, creemos que un subconjunto de pacientes termina con efectos neurológicos”.
Dieciocho meses después, en marzo de 2020, escribimos en la página de Opinión de The Wall Street Journal:
Recibimos un promedio de 45 nuevos pacientes de PFS al mes golpeando nuestra puerta digital de todo el mundo, un 462 % más desde 2018… Un número cada vez mayor de estos pacientes nos informa que Hims les recetó finasteride, virtualmente, Torres o romanas. Y prácticamente sin previo aviso de PFS.
Y hace tan solo siete meses, en un informe en este suministro de noticias titulado Primeras reacciones adversas de suicidio por suicidio agregadas a la etiqueta del producto Propecia de EE. UU., por mandato de la FDA, escribimos:
Más problemáticos, en términos de garantizar que todos los pacientes de EE. UU. que toman finasteride 1 mg o que estén considerando tomar finasteride 1 mg sean informados de inmediato de que la FDA ha reconocido que el medicamento podría precipitar el suicidio, son los servicios de telemedicina Big 3 cuyos negocios principales están al menos parcialmente dominados. por las ventas de finasteride.
Desde su fundación en 2017, Hims, Keeps y Ro (anteriormente Roman) han recaudado alrededor de $1300 millones en capital de riesgo… lo que les brinda amplios medios para dirigirse de manera agresiva a los hombres que buscan tratamientos para la caída del cabello. El problema es que, según una revisión realizada por la Fundación PFS del contenido digital de consumo de los tres telemédicos, ninguno de ellos [menciona las ADR de suicidio exigidas por la FDA].
 Roe v. vadear aguas no reguladas
Roe v. vadear aguas no reguladas
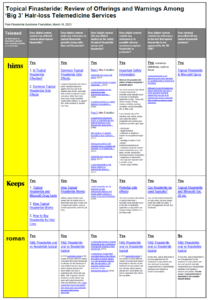
Ahora, con más informes en camino de pacientes con PFS que desarrollan la afección solo con finasterida tópica, hemos producido un complemento a esa investigación: Finasterida tópica: revisión de ofertas y advertencias entre los servicios de telemedicina para la pérdida de cabello de los ‘3 grandes’.
La observación más destacada es que, a diferencia de los competidores Hims y Keeps, Ro ha optado por no prescribir/vender productos de finasterida tópica. Su razón de ser es simple:
En este momento, la finasterida tópica no está aprobada por la FDA para el tratamiento de la pérdida de cabello de patrón masculino y debe ser especialmente formulada por una farmacia de compuestos y requiere receta médica. Por esta razón, la finasterida tópica compuesta no está disponible a través de Roman.
Keeps, mientras tanto, parece no poder decidir si la finasterida tópica es mejor o peor que la finasterida oral.
Por un lado, el único producto de su página principal es Finasteride Tópico y Minoxidil Gel, que se promociona así: “Cuidar el cabello nunca ha sido tan fácil. Obtenga dos productos clínicamente probados en un gel que se toma una vez al día”.
Por otro lado, su página de información sobre medicamentos tópicos de finasterida y minoxidil es solo de nombre. Aparte del término «finaserida tópica» en su título, la página no hace ninguna referencia a la finasterida tópica. Y los dos estudios clínicos relacionados con la finasterida citados en esa página se publicaron en 1998 y 1999, más de una década antes de que la finasterida tópica apareciera por primera vez en la literatura médica como una posible terapia para la alopecia androgénica (AGA).
Aún más extraño, otra página de Keeps, Cómo comprar finasteride para la pérdida del cabello, contiene una sección titulada «¿Se puede usar finasteride por vía tópica?» que dice, en parte:
Puede encontrar finasterida tópica a la venta en línea, pero debe saber que, a diferencia de la tableta, no está aprobada por la FDA para el tratamiento de la caída del cabello… Si salen a la luz más estudios positivos, la FDA podría considerar cambiar su postura sobre la finasterida tópica. Hasta entonces, sugerimos seguir con la versión oral, solo para estar seguros.
Así que la píldora es, ¿verdad? No tan rapido.
Cualquier posible paciente con finasterida que tenga los medios para buscar la información de prescripción (PI) aprobada por la FDA del medicamento encontrará un enlace en la página de Finasterida de Keeps. El problema es que, desde que llevamos a cabo nuestra Revisión de la Divulgación de ADR sobre Suicidalidad exigida por la FDA de EE. UU. hace cinco meses, Keeps actualizó esa página con la última versión de la PI, la que ahora enumera la «ideación y el comportamiento suicida» como una reacción adversa.
Es difícil imaginar una reacción adversa peor que el suicidio. Pero a partir de la «lógica» del contenido digital para el consumidor de Keeps, podría haber uno al acecho en cada botella de su Gel Tópico de Finasterida y Minoxidil.
En cuanto a Hims, vimos de primera mano su proceso de prescripción de finasterida tópica el mes pasado. Vale la pena agregar aquí, sin embargo, que la compañía de $ 2 mil millones promueve Topical Finasteride & Minoxidil Spray como su «favorito número 1 de los clientes» y el producto «más popular«.
 ¿Qué está pasando en Washington, DC?
¿Qué está pasando en Washington, DC?
Since the FDA does not comment on products under consideration for marketing approval (or no), revisamos el sitio web de la agencia en busca de pistas sobre el estado futuro de la finasterida tópica en los EE. UU. En cuanto a la vigilancia, encontramos dos casos:
• Hybrid Pharma LLC: una inspección de 2021 en esta instalación de externalización de Deerfield Beach, Florida (también conocida como instalación de compuestos) arrojó la siguiente observación:
Su centro de subcontratación no presentó un informe a la FDA en el momento del registro inicial como centro de subcontratación que identificara los medicamentos compuestos durante el período anterior de seis meses. Específicamente, los siguientes productos fueron compuestos y no identificados en sus informes: minoxidil al 5 %, tretinoína al 0,01 %, finasterida al 2,5 % solución tópica…
• Rx Unlimited Pharmacy: una inspección de 2022 en esta instalación de subcontratación de North Hills, California, arrojó la siguiente observación:
Desde mayo de 2022, su empresa produce formulaciones de productos farmacéuticos [ELIMINADO] (aerosol nasal, suspensión oral, soluciones orales y tópicas) utilizando [ELIMINADO] como ingrediente. En los últimos tres meses, su empresa entregó [ELIMINADO] recetas de pacientes con [ELIMINADO] como ingrediente. Por ejemplo, dispensó los siguientes productos farmacéuticos compuestos:
—Espuma de finasterida 0,2%
—Solución tópica de minoxidil al 6 %/finasterida al 0,2 %
Entonces, sabemos que la FDA está prestando atención a la producción y dispensación de productos de finasterida tópica. Pero según un informe actualizado por última vez el 14 de marzo de 2023, la finasterida se encuentra actualmente en evaluación como una «sustancia farmacológica a granel» para su uso en compuestos.
Cuando Roman Kulikov se enteró de que la finasterida tópica había sido aprobada en Alemania y Corea, inmediatamente dio un paso al frente para hablar en nombre de los pacientes con SPF en todo el mundo.
«Nos engañaron con la introducción de las pastillas de Propecia en 1997 y ahora, 26 años después, nos vuelven a engañar con estas cremas, geles y aerosoles de finasterida», dice la cocinera berlinesa de 32 años que ha sufrido de PFS desde 2015.
“Pensamos que las compañías farmacéuticas como Merck y Organon estaban en el negocio de hacer avanzar la ciencia, pero en realidad están en el negocio de hacer avanzar sus cuentas bancarias”, agrega.
Cada vez más desesperado por aliviar sus más de 40 síntomas de PFS, que van desde el encogimiento del pene hasta la ginecomastia, la pérdida de dientes, los niveles elevados de glucosa, la atrofia muscular y los cambios de humor extremos, hace tres años, Ro recurrió a Michael Zitzmann, MD, en el Centro de Salud Reproductiva. Medicina y Andrología en Münster.
“El paciente tomó finasteride durante 3 meses en 2015… El paciente teme que su pene desaparezca. A veces no hay sensación de la presencia de este órgano. Sin relación en este momento. No hay deseo de paternidad”, escribió el Dr. Zitzmann, cuya entrevista DAZ de 2018 se tituló Apuntando a los esteroides neuroactivos, en los registros médicos de Ro.
“Mis habilidades cognitivas han disminuido, mi coeficiente intelectual ha disminuido”, dice Roman. “Solía ser capaz de pensar en mis pies y manejar tareas complejas con facilidad. Pero ahora lucho incluso con los desafíos mentales más simples”.
 Qualquier persona que viva en los EE. UU. que sufra de PFS debe informar sus síntomas a la FDA de los EE. UU. Cualquier persona que viva fuera de los EE. UU. que sufra de PFS debe informar sus síntomas a la FDA de los EE. UU., así como a su autoridad reguladora de medicamentos (DRA) local, como se indica en nuestra página Informe sus efectos secundarios.
Qualquier persona que viva en los EE. UU. que sufra de PFS debe informar sus síntomas a la FDA de los EE. UU. Cualquier persona que viva fuera de los EE. UU. que sufra de PFS debe informar sus síntomas a la FDA de los EE. UU., así como a su autoridad reguladora de medicamentos (DRA) local, como se indica en nuestra página Informe sus efectos secundarios.
Finalmente, si usted o un ser querido sufre de PFS y se siente deprimido o inestable, no dude en comunicarse con la Fundación PFS lo antes posible a través de nuestra línea directa de atención al paciente: social@pfsfoundation.org
Gracias.
Noticias Relacionadas

